Растущий спрос на быстрый доступ к малым молекулам с новыми архитектурными решениями для высокопроизводительного скрининга предоставил сложные возможности химикам-синтетикам. Несмотря на значительные успехи в этой области, отсутствие систематических стратегий планирования библиотек было названо ограничивающим фактором в этом процессе. 1 Разнообразный синтез (DOS) 1 , 2 возник этот недостаток в качестве стимулирующей платформы для легкого производства нескольких строительных лесов 1 - 3 демонстрируя скелетное разнообразие. 2 , 4 Среди нескольких функций, которые определяют DOS, форвард-синтетический анализ 1 , 2 и функциональная группа (FG) спаривания 5 , 6 всплыли как важные инструменты. В частности, форвард-синтетический анализ фокусируется на всеобъемлющих стратегиях для создания нескольких каркасов за наименьшее количество возможных шагов, в то время как спаривание FG направлено на выборочное соединение функциональных групп из центрального функционализированного ядра, что приводит к быстрому созданию массива каркасов с минимальными шагами. Обе концепции лежат в основе стратегии «Построить / Пара / Пара (BCP)», предложенной Шрайбером и его сотрудниками. 6 Эта стратегия включает в себя «фазу сборки» для сборки хиральных строительных блоков, содержащих ортогональные наборы функциональных возможностей, подходящих для последующих фаз «сопряжения и сопряжения FG» на пути к массиву разнообразных строительных лесов. В связи с этим, интерес к получению султама с разнообразными скелетами для биологического скрининга послужил стимулом для названной стратегии циклизации спаривания FG, называемой «щелкни, щелкни, циклизуй», вплоть до пяти, шести, семи, восьми и девяти кольцевые сультамы. 7
Сульфонамиды долгое время ценились за их богатые биологические и химические характеристики и стали перспективным классом соединений для открытия лекарств. 8 Султамы (циклические сульфонамиды), хотя и не встречаются в природе, проявляют широкий спектр мощных биологических активностей. 9 , 10 Традиционно синтезы султама основывались на классических протоколах циклизации и ряде процессов, катализируемых переходными металлами, о которых недавно сообщалось. 10 В этом отношении винилсульфонамиды представляют собой возникающий хемотип с широким спектром реакционного потенциала для образования сультамов. Литературное превосходство показало их реактивность в Diels-Alder, 11 Черт возьми, 12 инициированное индием радикальное добавление, 13 и [3 + 2] циклоприсоединения. 14 Этот химический профиль дополняется недавней работой с использованием метатезиса с замыканием кольца (RCM), 10a , 15 внутримолекулярная циклизация окса-Михаэля и Бэйлиса-Хиллмана с образованием сультамов. 16 Взятые вместе, эти методы представляют возможности для реализации подходов DOS к новым sultams.
В основе названного подхода лежит легкое производство предшественников третичных винилсульфонамидов путем использования двух реакций «щелчка» 7 (). Эти две надежные реакции включают (i) винилсульфонилирование аминов и последующее алкилирование образующихся вторичных сульфонамидов или (ii) получение вторичного амина через отверстие эпоксида с амином с последующим винилсульфонилированием. Последующее спаривание FG в любом случае между винилсульфонамидным фрагментом A и FG B, C и D приводит к образованию сультамов различной архитектуры. 17 Альтернативно, использование третьей реакции, 7 реакция аза-Михаэля, позволяющая расширить схемы сопряжения FG и установить дополнительный элемент разнообразия. В целом, эти стратегии основаны на эффективных и разрозненных путях спаривания FG на третичных винилсульфонамидах для создания реакционных коллекторов, исходящих из одного стержня.
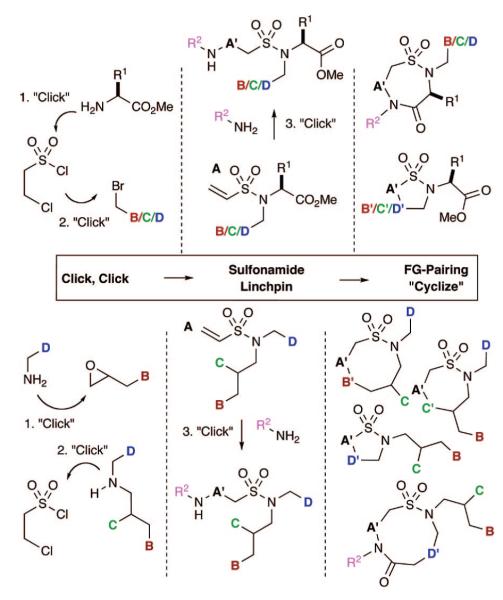
«Кликни, кликни, циклизируй» или «кликни, кликни, кликни, циклизуй» подход к скелетам с разнообразными сультамами.
Это исследование было начато с изучения нескольких путей спаривания FG между винилсульфонамидами и разрозненными функциональными группами, включая внутримолекулярную Heck, aza-Michael, 18 реакции метатезиса с замыканием кольца (RCEM), реакции Pauson-Khand (PK) и реакции хемоселективного окисления / Baylis-Hillman, как описано в. Эти методы устанавливают основу для общего подхода DOS, изложенного в Схемах, и, таким образом, умножение одного каркаса 3 может быть реализовано
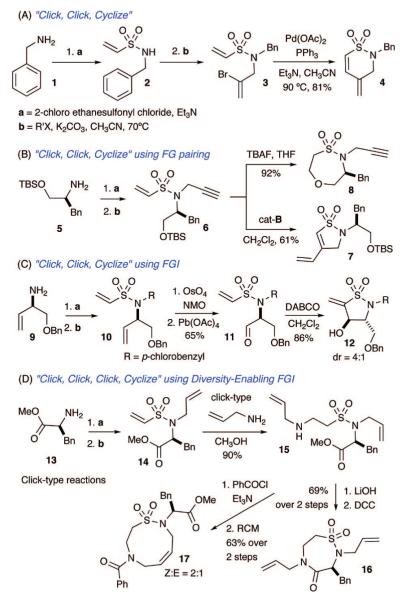
DOS через реакционные коллекторы «щелкни, щелкни, циклизируй»
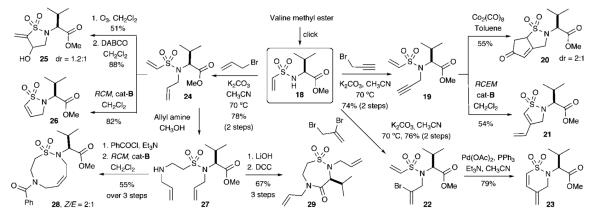
Реакционные коллекторы «щелкни, щелкни, циклизируй» с использованием FG-спаривания в пути к султамам с разнообразным скелетом
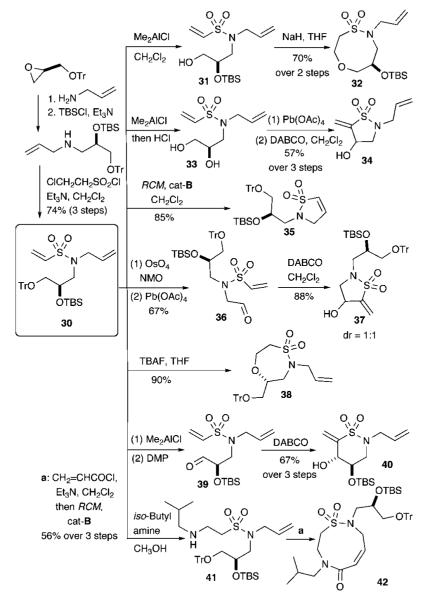
FG Соединение с Sultams с использованием FGI
Первый исследованный путь был начат с последовательности винилсульфонилирования / аллилирования, в результате которой был получен третичный винилсульфонамид 3 , который подвергается региоселективной внутримолекулярной циклизации 6- эндотрига Гека с получением δ -сульфама 4 с хорошим выходом (путь А). Этот путь подвержен изменениям как аминного компонента, так и партнера алкилирования, как показано на фиг.
Использование TBS-защищенного аминоспирта и пропаргилбромида в винилсульфонилировании / алкилировании соответственно дает третичный сульфонамидный линчпин 6 (путь B). Линчпин 6 вооружен для внутримолекулярного метатезиса энина с образованием сультама 7 , тогда как снятие защиты с TBAF инициирует внутримолекулярную циклизацию окса-Михаэля с получением 8 с выходом 92%.
Использование межконверсии FG (FGI) расширяет коллектор реакции, допуская новое событие сопряжения FG (путь C). В этом примере хемоселективное окисление аллильного фрагмента в присутствии электронодефицитного винилсульфонамида обеспечивает возможность циклизации FG-спаривания между альдегидным и винилсульфонамидным фрагментами с использованием внутримолекулярной реакции циклизации Байлиса-Хиллмана. В связи с этим последовательное винилсульфонилирование амина 9 и алкилирование дают винилсульфонамид 10 с хорошим выходом. Хемоселективное окисление с помощью OsO4 / NMO / Pb (OAc) 4 с последующей циклизацией Байлиса-Хиллмана, инициированной DABCO, дает γ- сультам 12 с выходом 86% (dr = 4: 1).
Четвертый путь использует реакцию аза-Майкла в последовательности реакций «щелкни, щелкни, щелкни, циклизируй», которая воздействует на амплитудный FGI электрофильного винилсульфонамида в нуклеофильный аминосульфонамид (путь D). Эта последняя концепция представляет собой этап, обеспечивающий разнообразие, и предлагает новый паттерн спаривания FG между нуклеофильным амином (NHR2) и остальными FG.
Хотя ранее сообщалось об использовании реакции аза-Михаэля на винилсульфонамиде, 18 его использование в синтезе сультама ограничено. 16 В этом исследовании было обнаружено, что 14 подвергается легкой реакции аза-Михаэля с получением сульфонамида 15 с превосходным выходом. Последующий основной гидролиз и внутримолекулярная лактамизация дают семичленный сультам 16 . Альтернативно, реакция с бензоилхлоридом, сопровождаемая RCM, дает девятичленный сультам 17 с выходом 63% ( Z / E = 2: 1).
Пути A-D, обозначенные в, могут быть легко интегрированы в стратегии DOS, как описано в Схемах и. Первая стратегия коллектора реакции DOS, которую мы исследовали, началась с готового винилсульфонамида 18, полученного из винилсульфонилирования метилового эфира валина с 2-хлорэтансульфонилхлоридом. Последующее алкилирование пропаргилбромидом, 2,3-дибромпропеном или аллилбромидом объединяет сульфонамидный стержень для трех центральных путей реакции. Они включают в себя (i) пропаргилирование до 19 с последующей внутримолекулярной циклизацией Паузона-Ханда с получением каркаса сультама 20 или RCEM с (IMesH2) (PCy3) - (Cl) 2Ru = CHPh (Grubbs cat-B) для получения сультама 21 , (ii ) аллилирование 18 2,3-дибромпропеном с выходом 22 с последующей региоселективной внутримолекулярной циклизацией Гека с получением сультама 23 с выходом 79% и (iii) аллилирование 18 с использованием аллилбромида с выходом 24 .
Этот последний путь аллилирования открывает три дополнительных реакционных пути для расширения общего реакционного коллектора DOS (). В первом способе используется селективное окисление озоном для получения альдегида для последующей внутримолекулярной циклизации Бэйлиса-Хиллмана, что дает γ- сультам 25 с выходом 88% с диастереоселективностью 1,2: 1. Второй маршрут использует RCM 24 с cat-B для получения γ- сультама 26 . Третий путь использует вышеупомянутую межмолекулярную реакцию аза-Михаэля винилсульфонамида 24 с получением β- аминосульфонамида 27 , что приводит к еще двум дополнительным синтетическим ответвлениям. Простое бензоилирование 27 с последующей RCM-реакцией дает девятичленный сультам 28 с выходом 55% ( Z / E = 2: 1). Альтернативно, гидролиз сульфонамида 27 и внутримолекулярное амидирование с использованием сочетания DCC дает семичленный сультам 29 . В целом, этот процесс дает в общей сложности семь различных строительных лесов Sultam в короткие сроки.
Вторая стратегия DOS была начата с винилсульфонамида 30 , в котором три функциональные группы включены в аминный компонент для спаривания FG. Семь синтетических маршрутов были разработаны. Первый использует хемоселективное снятие защиты с тритильной группы 30 с использованием Me2AlCl с последующим добавлением активированного NaH окса-Михаэля для получения сультама 32 с выходом 70% за две стадии (). Второй использует глобальное снятие защиты для получения диола 33 . Последующее окислительное расщепление с помощью Pb (OAc) 4 и циклизация Бэйлиса-Хиллмана дает сультам 34 с выходом 57% за три стадии. Третий пример включает RCM винилсульфонамида 30 с получением каркаса из султама 35 с выходом 85% с использованием cat-B. Альтернативно, селективное окисление концевого олефина в винилсульфонамиде 30 с последующей внутримолекулярной циклизацией Бэйлиса-Хиллмана дает султам 37 . Пятый пример демонстрирует легкую циклизацию окса-Михаэля, инициированную снятием защиты TBAF с получением каркаса сультама 38 с выходом 90%. Шестой пример включает селективное снятие защиты с тритила / окисление по Дессу-Мартину и внутримолекулярный Бейлис-Хиллман с получением сультама 40 с выходом 67% в течение трех стадий с диастереоселективностью> 20: 1. В седьмом и последнем примере используется межмолекулярная аза-реакция Михаэля с аллиламином с образованием β- аминосульфонамида 41 , который взаимодействовал с акрилоилхлоридом и подвергался RCM с cat-B с получением девятичленного кольцевого сультам-лактама 42 ( Z / E = 2: 1) с выходом 56% за три этапа. В целом, семь уникальных каркасов производятся в простых реакционных последовательностях.
Таким образом, мы сообщили о нескольких путях спаривания FG для получения сультамов на основе универсальных винилсульфонамидных линчпинов. Включение FGI, обеспечивающего разнообразие, расширяет коллекторы реакции DOS и расширяет область применения метода. Эти результаты в высшей степени поддаются для библиотечного производства, и постоянные усилия в порядке.